
8月25日,《科学》杂志发表了中国科学院生物物理研究所常文瑞/李梅研究组、章新政研究组与柳振峰研究组的最新合作研究成果。该项工作报道了豌豆光系统II-捕光复合物II超级复合物的高分辨率电镜结构,揭示了植物在弱光条件下进行高效捕光的超分子基础。
光合作用是地球上最为重要的化学反应之一。植物、藻类和蓝细菌进行的放氧型光合作用不仅为生物圈中的生命活动提供赖以生存的物质和能量,同时还维持着地球上的大气环境和碳氧平衡。对光合作用机理的研究不仅具有重要的理论意义,而且将为基于光合作用原理的应用研究提供具有启示性的方案。在高等植物中,光合作用的原初反应始于一个被称为光系统II的超分子机器,它能够捕获光能并将其用于驱动能量转换和在常温常压下裂解水分子。高等植物的光系统II是一个复杂的膜蛋白-色素超分子复合物,通常以二体形式存在,其每个单体包含了约30个蛋白亚基以及数百个色素分子和其它辅因子。为适应不同的外界光照条件,高等植物光系统II与外周的捕光复合物组装成多种不同形式的超级复合物。在适应弱光条件的植物叶片中,光系统II核心复合物的外侧结合了两种主要捕光复合物LHCII(根据亲和力的不同分为S-LHCII和M-LHCII)及三种次要捕光复合物CP29、CP26和CP24。这些捕光复合物与光系统II核心复合物组装形成C2S2M2型超级复合物,使其得以在弱光条件下高效地捕获光能并完成能量转换。C2S2M2型复合物是迄今为止在高等植物中能被稳定分离得到的最大的光系统II超级复合物。解析该复合物的完整结构对于人们认识其内部的亚基组成及排布方式、色素结合位置及相互取向和距离具有重要的科学意义。研究结果有助于深入理解植物高效捕获和传递光能的分子机理。
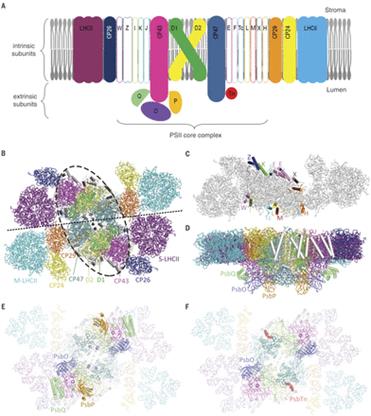
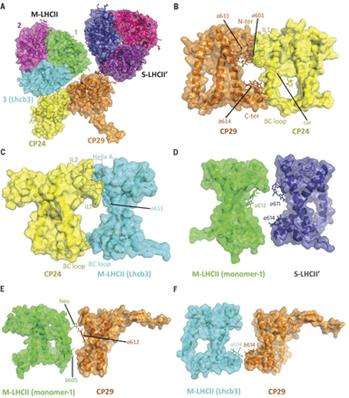
由生物物理所三个课题组组成的联合研究团队解析了处于两种不同条件下的豌豆C2S2M2超级复合物的单颗粒冷冻电镜结构,分辨率分别达到2.7埃和3.2埃,其中2.7埃分辨率的结构是目前世界上通过冷冻电镜单颗粒法解析获得的分辨率最高的膜蛋白结构。该项工作首次展示了植物C2S2M2型超级复合物的精确三维结构,该复合物总分子量达到140万道尔顿,是一个同源二聚体的超分子体系。两个结构中的每个单体分别包含了28或27个蛋白亚基、159个叶绿素分子、44个类胡萝卜素分子和众多的其它辅因子。该项工作首次解析了CP24和M-LHCII的结构,并指认了M-LHCII所特有的Lhcb3亚基;展示了不同外周捕光蛋白彼此之间以及它们与核心复合物之间相互识别和装配的位点和机制;在对豌豆C2S2M2超级复合物内部高度复杂的色素网络进行深入分析的基础上,揭示了外周天线捕获光能并向核心复合物传递能量的途径。同时,两种不同状态的C2S2M2结构的比较分析结果显示,超级复合物中的外周捕光复合物M-LHCII和CP24的结合位置可变,提示高等植物光系统II超级复合物可对环境条件的变化做出响应,通过整体结构的变化实现对捕光过程的调节。上述研究结果对于进一步在分子水平深入理解高等植物光系统II超级复合物中的能量传递和光保护机理具有重要意义。《科学》杂志在同期为该项研究工作配发了题为The complex that conquered the land 的评述。
李梅、章新政和柳振峰为论文的共同通讯作者,副研究员苏小东、助理研究员马军、博士魏雪鹏、副研究员曹鹏为共同第一作者。这是该团队继2016年在《自然》上报道菠菜C2S2型超级复合物的冷冻电镜结构之后的又一重要突破。该研究工作得到了中科院B类先导专项、中科院前沿科学重点研究项目、科技部重点研发计划、科技部973重大科学问题导向项目、国家自然科学基金的共同资助。数据收集和样品分析等工作得到了生物物理所生物成像中心、蛋白质科学研究平台等的大力支持和帮助。(来源:中国科学院生物物理研究所)
Structure and assembly mechanism of plant C2S2M2-type PSII-LHCII supercomplex
Abstract In plants, the photosynthetic machinery photosystem II (PSII) consists of a core complex associated with variable numbers of light-harvesting complexes II (LHCIIs). The supercomplex, comprising a dimeric core and two strongly bound and two moderately bound LHCIIs (C2S2M2), is the dominant form in plants acclimated to limited light. Here we report cryo–electron microscopy structures of two forms of C2S2M2 (termed stacked and unstacked) from Pisum sativum at 2.7- and 3.2-angstrom resolution, respectively. In each C2S2M2, the moderately bound LHCII assembles specifically with a peripheral antenna complex CP24-CP29 heterodimer and the strongly bound LHCII, to establish a pigment network that facilitates light harvesting at the periphery and energy transfer into the core. The high mobility of peripheral antennae, including the moderately bound LHCII and CP24, provides insights into functional regulation of plant PSII.
原文链接:http://science.sciencemag.org/content/sci/357/6353/815.full.pdf



